Cho 2,4(g) kim loại Mg phản ứng với 250 ml dung dịch axit HCl 1M.
a,tính thể tích khí H2 thu đc(đktc)
b,tính nồng độ mol các chất trong dung dịch sau phản ứng
(cho:Mg=24,H=1,Cl=35,5)
Cho 250ml dung dịch HCl 0,2M thì tác dụng vừa hết với kim loại magie.
a. Tính thể tích khí hidro thoát ra ở đktc?
b. Tính nồng độ mol của magie clorua trong dung dịch sau phản ứng? (Mg=24; Cl=35,5; H=1)
a) nHCl = 0,25.0,2 = 0,05 (mol)
PTHH: Mg + 2HCl --> MgCl2 + H2
0,05-->0,025->0,025
=> VH2 = 0,025.22,4 = 0,56 (l)
b) \(C_{M\left(MgCl_2\right)}=\dfrac{0,025}{0,25}=0,1M\)
Cho 8,9g Mg, Zn tác dụng với 200g dung dịch HCL xM. Sau phản ứng thu được 2,24 l khí H2 ở đktc?
a) Viết PTHH
b) Tính % khối lượng từng kim loại trong hỗn hợp ban đầu ?
c) Tính nồng độ mol của HCL đã dùng?
d) Tính nồng độ mol các chất thu đc sau phản ứng?
Giúp mình nhanh với:((
Cho 5,6 gam kim loại Fe tác dụng với 150 ml dung dịch HCl. Sau phản ứng thu được muối sắt (II) clorua (FeCl2) và khí H2. a. Tính nồng độ mol dung dịch HCl đã phản ứng và thể tích khí H2 (ở đktc) sau phản ứng? b. Cần dùng bao nhiêu lít dung dịch NaOH 2M để phản ứng hết với muối sắt (II) clorua (FeCl2) thu được ở trên
Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
____0,1______0,2_____0,1____0,1 (mol)
a, \(C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}\left(M\right)\)
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\)
Theo PT: \(n_{NaOH}=2n_{FeCl_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{NaOH}=\dfrac{0,2}{2}=0,1\left(l\right)\)
Cho 3,6 gam kim loại Mg vào 250 ml dung dịch FeCl3 1M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn và dung dịch X. Tính m và nồng độ mol của các chất trong dung dịch X ( xem như thể tích dung dịch sau phản ứng không đổi) ?
nMg = 3,6/24 = 0,15 mol; nFeCl3 = 0,25.1 = 0,25 mol
Mg + 2FeCl3 → MgCl2 + 2FeCl2
0,125dư 0,025←0,25 → 0,125 → 0,25 (mol)
Mg + FeCl2 → MgCl2 + Fe
0,025→0,025 →0,025→0,025 (mol)
Vậy chất rắn sau phản ứng là Fe: nFe = 0,025 mol
=> m = mFe = 0,025.56 = 1,4 (gam)
Dung dịch X sau phản ứng gồm:
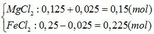
Nồng độ của các chất trong dung dịch X:
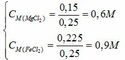
Cho 4.8(g) magie phản ứng vừa đủ với 200 ml dung dịch HCI sau phản ứng thu được dung dịch magie clorua và khi hidro a. Viết PTHH b. Tính nồng độ mol dung dịch axit đã dùng c. Tính thể tích khí hiđro bay ra ở đktc. Cho: Mg=24, H=1, CI=35.5, S-32, 0=16, S=32, Na=23)
\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{4.8}{24}=0,2mol\)
đổi 200 ml = 0,2 l
PTHH: Mg + 2HCl \(\rightarrow\) MgCl2 + H2
TL; 1 2 1 1
mol: 0,2 \(\rightarrow\) 0,2 \(\rightarrow\) 0,2
b. \(C_{M_{ddHCl}}=\dfrac{n_{HCl}}{V_{dd_{HCl}}}=\dfrac{0,2}{0,2}=1M\)
\(c.V_{H_2}=n_{H_2}.22,4=0,2.22,4=4,48l\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
a) PTHH : \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b) \(n_{HCl}=2n_{Mg}=0,4\left(mol\right)\Rightarrow C_{MddHCl}=\dfrac{0,4}{0,2}=2M\)
c) \(n_{Mg}=n_{H2}=0,2\left(mol\right)\Rightarrow V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
Câu 1: Cho Mg tác dụng vừa đủ với 200 ml dung dịch HCl 1M , sau phản ứng thu được dung dịch X và khí H2.
a) viết PTHH xảy ra.
b) tính thể tích khí H2 thu được ở đkc.
c) coi thể tích dung dịch thay đổi không đáng kể, hãy tính nồng độ mol của các chất có trong dun dịch X
Câu 2: Cho 1.2 gam magnesium tác dụng với dung dịch HCl 2M (hiệu suất phản ứng 100%) để điều chế khí hydrogen
a) Viết PTHH của phản ứng xảy ra.
b) Tính thể tích khí hydrogen thu được ở đkc.
c) Tính thể tích dung dịch HCl cần dùng.
d) Tính nồng độ mol dung của dung dịch MgCl2 thu được sau phản ứng (coi thể tích dung dịch thay đổi không đáng kể
Câu 1
\(a)PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\
b)200ml=0,2l\\
n_{HCl}=0,2.1=0,2mol\\
n_{H_2}=n_{MgCl_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}\cdot0,2=0,1mol\\
V_{H_2}=0,1.24,79=2,479l\\
c)C_{M_{MgCl_2}}=\dfrac{0,1}{0,2}=0,5M\)
Câu 2
\(a)PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\
b)n_{Mg}=\dfrac{1,2}{24}=0,05mol\\
n_{H_2}=n_{MgCl_2}=n_{Mg}=0,05mol\\
V_{H_2}=0,05.24,79=1,2395l\\
c)n_{HCl}=2n_{Mg}=2.0,05=0,1mol\\
V_{ddHCl}=\dfrac{0,1}{2}=0,05l\\
d)C_{M_{MgCl_2}}=\dfrac{0,05}{0,05}=1M\)
Cho 2,4 g kim loại Mg tác dụng vừa đủ với 400 ml dung dịch axit clohiđric ? a, viết phương trình hóa học xảy ra b, tính thể tích khí Hiđro thu được trong điều kiện tiêu chuẩn c, tính nồng độ mol của dung dịch muối tạo thành sau khi phản ứng biết rằng thể tích của dung dịch thay đổi không đáng kể
Hoà tan hoàn toàn 13 gam Zn cần dùng 200ml dung dịch HCL Viết PTHH của phản ứng Tính thể tích H2 thu đc ở đktc? Tính nồng độ mol của dung dịch HCl đã dùng ? Cho biết: Zn=65;Cl=35,5;O=16;Cu=64;Fe=56,Mg=24,Na=40
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2}=n_{Zn}=0,2\left(mol\right)\\n_{HCl}=2n_{Zn}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(C_{M_{HCl}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
a) Mg + 2HCl → MgCl2 + H2
b) nMg =\(\dfrac{14,4}{24}\)=0,6 mol => nH2 = nMg= 0,6 mol <=> V H2 = 0,6.22,4 = 13,44 lít
c) nHCl = 2nMg = 1,2mol => mHCl = 1,2.36,5 = 43,8 gam
=> C%HCl = \(\dfrac{43,8}{200}.100\) =21,9%